Nanoteknoloji ile Ağız Biyofilmlerinde Hedefli Antimikrobiyal Salımı
Ne Oldu?
International Journal of Oral Science dergisinde yayınlanan kapsamlı bir derleme çalışması, ağız içi biyofilmlerin dinamik özelliklerine yanıt veren ve antimikrobiyal yüklü nanoyapıların potansiyelini inceledi. [1]
Çalışma, pH değişikliklerine, oksijen seviyesine (hipoksi) ve bakteriyel enzimlere duyarlı nanopartiküllerin, geleneksel antimikrobiyallere kıyasla ağız biyofilmlerine daha etkili nüfuz edebildiğini ve bu bölgelerde antimikrobiyalleri kontrollü şekilde serbest bırakabildiğini ortaya koydu. [1]
Neden Önemli?
Ağız Biyofilmlerinin Karmaşık Yapısı
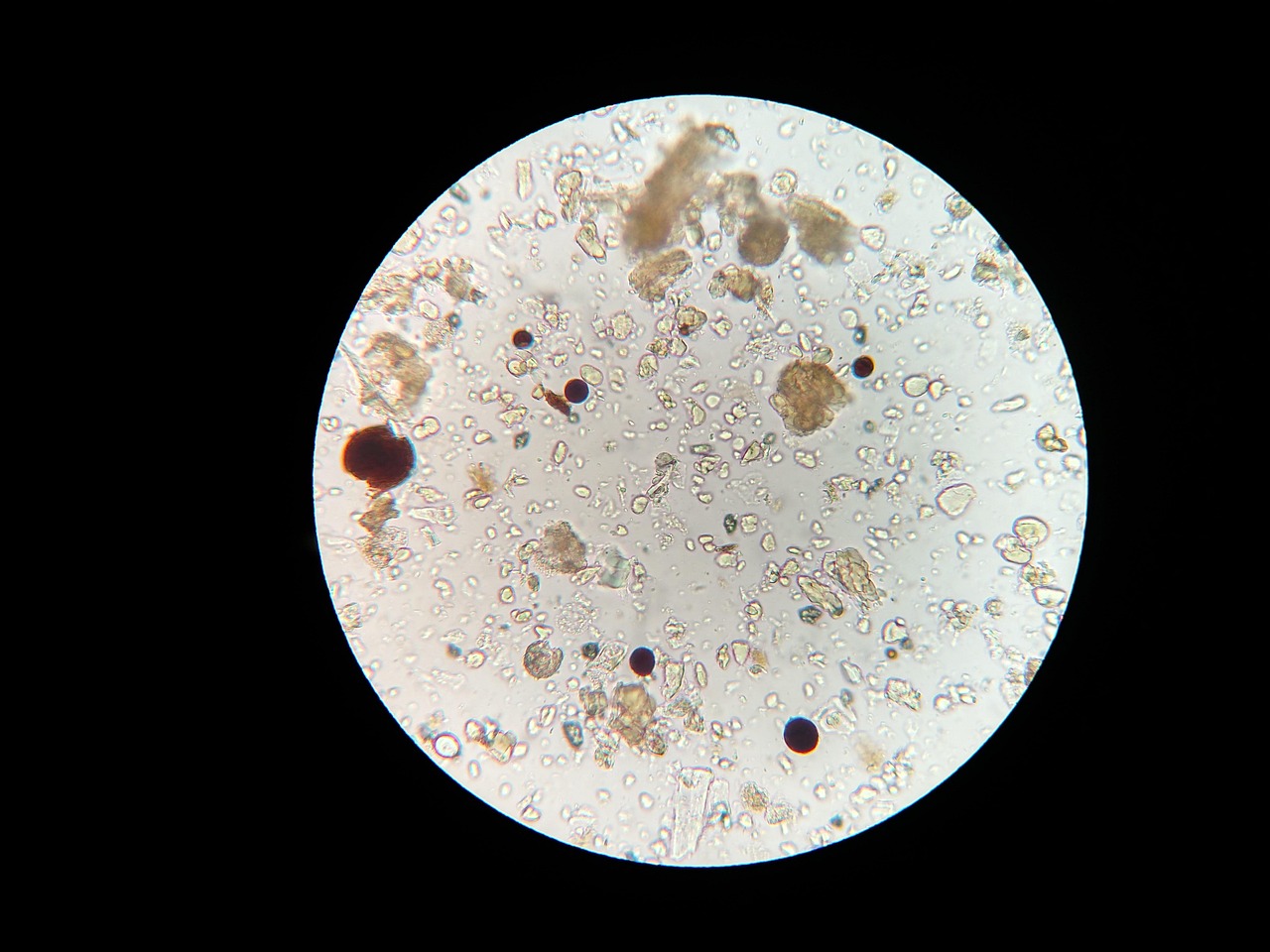
Ağız biyofilmleri, 500'den fazla bakteri türünün bir arada yaşadığı, ekstraselüler polimerik maddelerle (EPS) çevrili karmaşık yapılardır. [1] Bu biyofilmler iki ana kategoride incelenir:
Diş üstü (supra-gingival) biyofilmler:
- Tükürük ile çevrelenmiş
- Yemek sonrası pH 5'in altına düşebilen asidik ortam
- Çürük oluşumundan sorumlu
- Streptococcus mutans gibi patojenler içerir [1]
Diş eti altı (sub-gingival) biyofilmler:
- Dişeti oluğu sıvısı ile çevrelenmiş
- Hafif alkali ortam
- Periodontitis ve peri-implantitis nedeni
- Porphyromonas gingivalis gibi patojenler barındırır [1]
Geleneksel Antimikrobiyallerin Sınırlılıkları
Mevcut ağız antimikrobiyalleri (klorheksidin, triclosan, uçucu yağlar) önemli kısıtlamalara sahiptir:
- Biyofilm matrisine yetersiz penetrasyon
- Biyofilmin derin katmanlarındaki bakterilere ulaşamama
- Uzun süreli kullanımda yumuşak doku tahrişi
- İlaç direnci gelişimi riski [1]
1683 yılında Antonie van Leeuwenhoek'in gözlemlediği gibi, ağzını yıkamak için kullandığı sirkenin sadece biyofilmin üst katmanlarındaki mikroorganizmaları öldürebildiğini not etmesi, bu sorunun 300 yılı aşkın süredir devam ettiğini göstermektedir. [1]
Biyofilm-Duyarlı Nanopartiküller Nasıl Çalışır?
Kimyasal Yapı ve Mekanizma
Çalışmada incelenen nanopartiküller, genellikle 100 nm çapında olup, biyofilmlerdeki su dolu kanallara girebilecek boyuttadır. [1]
Üç ana uyaran tipine yanıt verirler:
-
pH-duyarlı nanopartiküller:
- Nötr pH'da negatif yüklü
- Asidik ortamda pozitif yüke dönüşür
- Amino grupları içeren yapılar (PEGylated-poly(amino esterler)) kullanır [1]
-
Hipoksi-duyarlı nanopartiküller:
- Oksijensiz ortamda aktive olur
- Nitrobenzil veya azobenzene grupları içerir
- İndirgenme sonucu pozitif yük kazanır [1]
-
Enzim-duyarlı nanopartiküller:
- Bakteriyel enzimler tarafından parçalanır
- Lipaz-duyarlı ester bağları içerir
- Proteaz-duyarlı peptit çapraz bağlayıcılar kullanır [1]
Biyofilme Nüfuz ve Birikim Mekanizması
Monte Carlo simülasyonları ve deneysel çalışmalar, bu nanopartiküllerin biyofilmlere nasıl nüfuz ettiğini göstermiştir:
- Negatif yüklü nanopartiküller biyofilm kanallarına girebilir ancak kanal duvarlarından elektrostatik itilme nedeniyle kolayca yıkanır
- pH veya hipoksiye yanıt vererek pozitif yüke dönüşen nanopartiküller, negatif yüklü kanal duvarlarına elektrostatik çekim ile yapışır
- Bu yapışma, nanopartiküllerin biyofilm içinde kalıcı birikim göstermesini sağlar [1]
10 günlük Staphylococcus aureus biyofilmlerinde yapılan deneylerde:
- pH-duyarlı nanopartiküller biyofilmin üst 20 µm'lik bölgesinde birikti
- Hipoksi-duyarlı nanopartiküller 20 µm'den derin bölgelerde toplandı
- Her iki uyarana duyarlı nanopartiküller tüm biyofilm derinliğinde yüksek birikim gösterdi [1]
Antimikrobiyal Salım ve Etkinlik
Kontrollü Salım Avantajları
Nanopartiküller iki tip salım gösterir:
İstenmeyen sızıntı (tükürükte):
- pH-duyarlı miseller: %69 sızıntı (pH 7.4'te)
- Hipoksi-duyarlı miseller: 4 kat daha az sızıntı
- Enzim-duyarlı miseller: Lipaz yokluğunda neredeyse sıfır sızıntı [1]
İstenen salım (biyofilm içinde):
- pH 5.5'te %84 klorheksidin salımı
- Hipoksik koşullarda 4 kat artmış siprofloksasin salımı
- Lipaz varlığında 25 saat içinde %100 triclosan salımı [1]
Yumuşak Doku Güvenliği
İnsan oral keratinositleri üzerinde yapılan in vitro çalışmalarda:
- 15.625 µg/mL klorheksidin konsantrasyonunda, nanopartikül yüklü form serbest klorheksidine kıyasla %40 daha yüksek hücre canlılığı sağladı
- Bu, biyofilm içinde yüksek antimikrobiyal konsantrasyonuna ulaşılırken, yumuşak dokuların daha az hasara uğradığını gösterir [1]
Preklinik Kanıtlar
In Vitro Çalışmalar
Çalışmalar çoğunlukla tek türlü biyofilmler (S. mutans, S. aureus) üzerinde yapılmıştır. [1]
Önemli bir çalışmada, insan mikrobiyom kaynaklı biyofilmler kullanılarak:
- pH-duyarlı, klorheksidin yüklü poli(DMAEMA-co-HEMA) misellerin çürük önleyici potansiyeli gösterildi
- 16S rRNA dizileme ile tür tanımlaması yapıldı [1]
In Vivo Hayvan Çalışmaları
S. mutans ile aşılanan sıçanlarda:
- pH-duyarlı Farnesol yüklü p(DMAEMA) blok kopolimer miseller kullanıldı
- Çürük lezyonlarının sayısı ve şiddeti yaklaşık 4 kat azaldı
- Serbest Farnesol çözeltisine kıyasla belirgin koruyucu etki [1]
Mikrobiyom Düzenleme Potansiyeli
Preklinik çalışmalar, pH-duyarlı nanopartiküllerin:
- Özellikle çürük yapıcı S. mutans'ı seçici olarak elimine edebildiğini
- Zararsız kommensal bakterilerin baskın hale gelmesine izin verdiğini
- Mikrobiyom kompozisyonunu daha sağlıklı bir dengeye doğru düzenlediğini göstermiştir [1]
Klinik Kanıtlar
İnsan Çalışması
Şu ana kadar sadece bir klinik çalışma mevcuttur:
Ortodontik hastalarda yapılan ex vivo çalışma:
- Braketler etrafında in vivo oluşan diş üstü biyofilm toplandı
- Triclosan yüklü, dual enzim ve pH-duyarlı misellerle ex vivo tedavi edildi
- Toplam Koloni Oluşturan Birim (CFU) sayısı değişmedi
- S. mutans sayısında anlamlı azalma gözlendi
- Bu, asidojenik patojenlerin seçici eliminasyonunu gösterir [1]
Üç Ana Klinik Fayda Potansiyeli
Preklinik çalışmalar, biyofilm-duyarlı antimikrobiyal nanopartiküllerin geleneksel moleküler antimikrobiyallere kıyasla üç önemli avantajını işaret etmektedir:
- Gelişmiş biyofilm içi antibakteriyel aktivite
- Yüksek biyofilm içi antimikrobiyal konsantrasyonu ile azaltılmış yumuşak doku hasarı
- Oral mikrobiyom kompozisyonunun daha sağlıklı bir yapıya doğru düzenlenmesi [1]
Sınırlamalar ve Gelecek Yönelimler
Mevcut Kısıtlamalar
- Çoğu çalışma tek türlü biyofilmler kullanmış
- Hayvan oral mikrobiyomu insan mikrobiyomundan farklı
- Ağız içi pH dalgalanmaları çoğu modelde yok
- Klinik doğrulama çok sınırlı
- Hipoksi-duyarlı nanopartiküller için hiç klinik çalışma yok [1]
Gelecek Araştırma İhtiyaçları
Derleme, şu konuların araştırılması gerektiğini vurgulamaktadır:
- Çok türlü insan mikrobiyom kaynaklı biyofilm modelleri kullanımı
- Uzun süreli klinik çalışmalar
- Periodontitis tedavisinde hipoksi-duyarlı nanopartiküllerin değerlendirilmesi
- Peri-implantitis gibi biyomateryal ilişkili enfeksiyonlarda etkinlik
- Güvenlik profili ve yan etkilerin kapsamlı değerlendirilmesi [1]
Sonuç
Bu kapsamlı derleme, uyaran-duyarlı, antimikrobiyal yüklü nanopartiküllerin ağız biyofilm kontrolü ve mikrobiyom restorasyonu için önemli bir potansiyele sahip olduğunu göstermektedir. [1]
Özellikle pH ve hipoksi-duyarlı sistemler, ağız biyofilmlerinin dinamik özelliklerinden yararlanarak:
- Hedefli antimikrobiyal salımı
- Gelişmiş biyofilm penetrasyonu
- Azaltılmış yumuşak doku toksisitesi
- Mikrobiyom dengesinin korunması sağlayabilir [1]
Ancak, bu teknolojinin klinik uygulamaya geçmesi için daha fazla insan çalışmasına ihtiyaç vardır. [1]
Önemli Not: Bu teknoloji henüz deneysel aşamadadır ve klinik kullanım için onaylanmamıştır. Ağız sağlığı sorunlarınız için mutlaka diş hekiminize danışın.